par Fabienne Maleysson, Perrine Vennetier, Gabrielle Théry
Médicaments périmésEncore actifs longtemps après
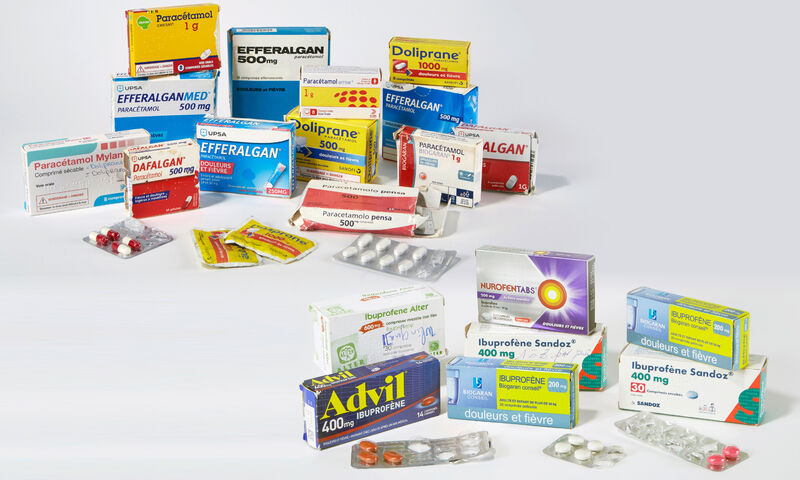
Notre analyse de 30 médicaments périmés montre qu’ils gardent leur efficacité des années après la date limite. Des délais rallongés permettraient de limiter le gaspillage et le choc des pénuries.
Nos analyses - 8 médicaments sur 10 gardent 90 % d’efficacité
Sur 30 échantillons périmés pour la plupart depuis des années, la teneur en principe actif est restée stable.
Nous avons récolté auprès de consommateurs, puis fait analyser, en juin 2024, par un laboratoire spécialisé 20 comprimés, gélules ou sachets de paracétamol (périmés entre 1992 et 2023) et 10 d’ibuprofène (périmés entre 2015 et mars 2024).
Seuls trois échantillons de chaque groupe contiennent moins de 90 % de la quantité affichée de principe actif (par exemple, moins de 900 mg de paracétamol pour un Doliprane 1 g). Les pires résultats : 84 % pour le paracétamol (date limite 2018) et 82 % pour l’ibuprofène (date limite 2022).
Les plus vieux ne sont pas toujours les moins dotés. De même, les conditions de conservation – du placard dans un endroit sec et tempéré à la boîte à gants d’une voiture en passant par une salle de bains à l’atmosphère chaude et humide – ne sont pas reliées au taux de substance active restante. Un stockage dans des conditions idéales n’a pas toujours permis une meilleure conservation qu’un traitement plus négligent.
Surpris ? Pas du tout. Lorsque les résultats d’analyse nous sont parvenus, indiquant que la majorité des médicaments supposés périmés étaient encore efficaces, nous avons tout simplement été confortés dans notre conviction. Car depuis des lustres, on sait que la date limite inscrite sur les boîtes ne signe pas l’arrêt de mort de leur contenu. Plusieurs équipes de chercheurs l’avaient déjà montré. Par exemple, des scientifiques allemands ont analysé, en 2018, neuf ampoules de diverses spécialités pharmaceutiques fabriquées plus de 40 ans auparavant et conservées sur les étagères d’un institut de recherche. Cinq d’entre elles renfermaient plus de 95 % du principe actif, dont une, « âgée » de 53 ans, atteignait les 99,3 %. Leurs collègues californiens avaient déniché, dans les recoins d’une officine, des boîtes a priori inutilisables depuis 28 à 40 ans. À l’arrivée, dans 12 cas sur 14, il subsistait plus de 90 % de substance active. Toutefois, ces deux expériences restent d’une ampleur limitée.
Aux États-Unis, des tests de stabilité
Ce n’est pas le cas du projet lancé, en 1986, sous le nom de « Programme d’extension des durées de conservation » par les autorités américaines. Elles gardent en permanence des stocks de médicaments susceptibles d’être employés par l’armée, ou par les populations civiles en cas d’événement exceptionnel (épidémie, attaque terroriste, etc.). Pour éviter de devoir les remplacer trop souvent, elles ont décidé de les soumettre régulièrement à des tests de stabilité et de repousser, le cas échéant, leur date limite. Ces tests comprennent non seulement la quantification du principe actif, mais aussi une analyse complète incluant notamment d’éventuels produits de dégradation, potentiellement toxiques.
Vingt ans après la mise en place du programme, la Food and Drug Administration (FDA, autorité chargée des médicaments aux États-Unis) publiait un bilan éloquent sur plus de 3 000 lots composés de quelque 120 catégories de traitements : 88 % d’entre eux ont pu voir leur durée de vie s’allonger d’au moins un an, avec une extension moyenne de 5 ans et demi ! Des spécialités courantes ont bénéficié d’un sursis non négligeable : l’amoxicilline, un antibiotique présent dans l’Augmentin ou le Clamoxyl (prolongation moyenne de 23 mois), le sérum physiologique (6 ans), la Bétadine (idem), le mélange paracétamol-pseudoéphédrine typique des médicaments anti-rhume (2 ans), etc.
Comment expliquer ces résultats ? Quand un laboratoire met un médicament sur le marché, il doit fournir aux autorités de santé les données de stabilité propres à justifier la durée d’utilisation à laquelle il aspire pour son produit. À cette fin, il procède à des tests à la fois dans les conditions normales sous nos climats (25 °C et 60 % d’humidité) et en conditions extrêmes (jusqu’à 40 °C et 75 % d’humidité). « Cela nous procure des informations utiles sur la cinétique de dégradation et le comportement du produit dans le temps », détaille-t-on à l’Agence nationale de sécurité du médicament (ANSM). Pour la plupart des spécialités, la teneur en principe actif doit être comprise entre 95 % et 105 % pendant toute la durée de vie, du moins en Europe. La FDA, elle, fixe généralement le seuil à 90 %. C’est donc bien que cette limite n’est pas synonyme d’inefficacité (1). En pratique, les industriels ne postulent le plus souvent qu’à une durée de vie de trois ans. Mais elle correspond davantage à un choix économique qu’à une réalité technique. En clair, si la date de péremption garantit l’intégrité du médicament avant cette échéance, elle ne signifie aucunement qu’il deviendra inefficace ou dangereux après !
D’inutiles dépenses
Outre l’absurdité environnementale qui consiste à jeter pléthore de produits parfaitement utilisables, ces dates de péremption trop courtes engendrent des montants faramineux de dépenses inutiles. Au détriment des consommateurs, quand ils achètent leurs médicaments de leur propre chef, de la Sécurité sociale, quand ils le font après une prescription, mais aussi de tous les établissements hospitaliers. Le coût total est colossal : un hôpital de taille moyenne situé à Boston (États-Unis) a calculé qu’il jetait pour 200 000 $ de boîtes chaque année. La question de l’extension des durées de vie se pose avec encore plus d’acuité lorsque les pénuries se multiplient, comme cela a été le cas ces dernières années. Début 2023, c’est le paracétamol qui manquait, un an après, c’était au tour de l’amoxicilline pédiatrique, et l’ANSM indiquait, en janvier dernier, que « toutes les classes de médicaments [étaient] concernées par les ruptures de stock ou les risques de ruptures ». Si les causes en sont multiples, il semble qu’un minimum d’anticipation couplée à une prolongation des durées de vie pourrait apporter une partie de la solution.
Toutes ces considérations, le gouvernement les prend depuis peu en compte dans le cadre de la « Planification écologique du système de santé ». L’ANSM travaille avec les firmes pharmaceutiques afin de les inciter à retarder les dates de péremption. Des discussions sont engagées avec leurs représentants. Pour l’instant, d’après l’agence, ceux-ci expriment une réticence liée à l’apparence des emballages : selon eux, une durée de vie de cinq ans, par exemple, ne permettrait pas de maintenir une esthétique idéale et le respect du traitement risquerait d’en souffrir. Pourtant, s’il y a un lien entre le conditionnement et ce dernier, il tient plutôt à la difficulté de manipulation ou à la taille des caractères qu’à l’aspect plus ou moins « joli » ! C’est du moins ce qui ressort d’un rapport de l’Académie de médecine paru en 2015. Espérons donc que cet argument quelque peu fallacieux sera vite abandonné face à l’ampleur des enjeux.
À nous de jouer !
Et nous, consommateurs, comment devons-nous gérer nos armoires à pharmacie ? D’abord, pour éviter les surstocks, cessons de nous faire délivrer un médicament sous le seul prétexte qu’il figure sur une ordonnance, sans vérifier que l’on en a déjà à la maison. On rangera ses réserves non pas dans la salle de bains, mais à l’abri de la chaleur, de la lumière et de l’humidité, même si certains comprimés tiennent vaillamment le coup dans des conditions moins orthodoxes (lire l’encadré ci-dessous). Les liquides dont le flacon est ouvert – tels que les collyres – n’ont qu’une espérance de vie limitée. Idem concernant les pommades, pour lesquelles une hygiène scrupuleuse dans la manipulation est en outre nécessaire. Prudence également quand l’aspect du médicament a changé. Si sa couleur est altérée, sa texture, modifiée – comprimé effrité, par exemple –, ou bien s’il dégage une odeur inhabituelle, notamment dans le cas des formes liquides et crémeuses, il ne faut pas l’utiliser. L’aspirine aussi peut se dégrader facilement. On s’abstiendra si, après péremption, elle a changé d’aspect ou d’odeur.
Sous réserve de respecter ces consignes, consommer un médicament périmé n’engendre a priori qu’un risque : celui d’une efficacité un peu amoindrie. Comme l’a remarqué la Société de pneumologie de langue française en 2016, dans un article sur la question : « Aucun rapport faisant état d’une toxicité humaine due à l’ingestion, à l’injection ou à l’application topique d’un médicament actuel après sa date de péremption n’a été publié. » De fait, l’ANSM, à qui nous avons demandé si elle avait eu connaissance, via la pharmacovigilance, de cas d’effets indésirables dus à la consommation de produits périmés ne nous a pas répondu malgré un délai de 10 jours et plusieurs relances. Un silence qui en dit long.
(1) Seuls les « médicaments à marge thérapeutique étroite », délivrés sur ordonnance, imposent une teneur précise.
Paracétamol - Deux cas extrêmes
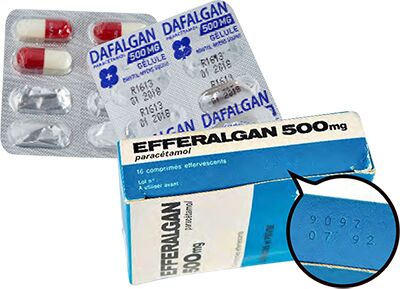
Ce sont les deux exemples les plus révélateurs de notre échantillonnage. Ces comprimés d’Efferalgan attendaient sagement dans un placard depuis au moins 35 ans. Leur propriétaire, Marie-Thérèse, 101 ans aux prunes, avait à peine entamé la boîte, elle qui a horreur de « se droguer », comme elle dit. De là à conclure que la sobriété pharmaceutique conserve… Toujours est-il que plus de trois décennies après leur date de péremption, fixée à juillet 1992, ces cachets contenaient encore 100 % de principe actif ! En comparaison, ces Dafalgan, périmés en janvier 2018, avaient connu une vie de patachon : glissés dans la poche d’un sac de randonnée, ils avaient supporté plusieurs jours de canicule en plein soleil, un orage mémorable, des averses en nombre, des journées à 4 ou 5 °C, et vécu le plus clair de leur temps dans une cave quelque peu humide. Mais plus de six ans après leur date limite, ils affichaient encore 95 % de paracétamol.
Fabienne Maleysson
Perrine Vennetier
Gabrielle Théry
Rédactrice technique
Lire aussi