par Anne-Sophie Stamane
ThyroïdeUn changement de formule houleux
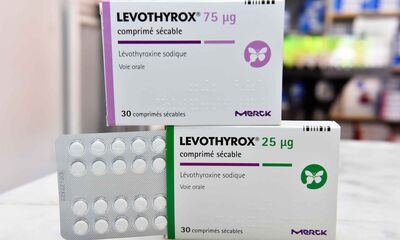
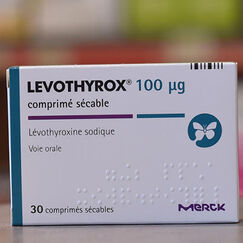
Une insuffisance ou une ablation de la thyroïde impose souvent un traitement à vie par lévothyroxine (Levothyrox des laboratoires Merck). Le médicament vient de changer de formulation. De nombreux patients se plaignent d’effets indésirables handicapants.
Maux de ventre, nausées, vertiges, fatigue, douleurs musculaires, irritabilité, voire asthme sévère : nombreux sont les effets indésirables rapportés suite au changement de formulation, en avril dernier, du Levothyrox (lévothyroxine), un médicament prescrit suite à une ablation de la thyroïde ou en cas d’insuffisance de cette glande. Au point qu’une pétition signée par 70 000 utilisateurs réclame le retour à l’ancienne composition ! Et qu’un numéro vert a dû être mis en place par l’Agence nationale de sécurité du médicament (ANSM) : le 0800 97 16 53 est accessible du lundi au vendredi, de 9 h à 17 h.
Rien n’a été modifié, pourtant, au niveau de la molécule active : les comprimés contiennent toujours les mêmes quantités de lévothyroxine. Ce sont les excipients qui ont changé : par souci de stabilité du médicament, et à la demande de l’ANSM, le laboratoire Merck a remplacé le lactose par du mannitol et de l’acide citrique.
Pour la grande majorité des trois millions de patients qui prennent ce produit quotidiennement, la transition n’a pas posé de problème. Mais il se peut que, pour une partie d’entre eux, le changement ait fait légèrement varier l’absorption de la molécule par l’organisme. Or, quelques microgrammes en plus ou en moins, s’agissant d’une hormone, sont susceptibles d’avoir un impact sensible.
En pratique, les personnes chez qui le nouveau Levothyrox entraîne des effets indésirables inhabituels et handicapants doivent consulter leur médecin. Il ne faut surtout pas stopper brutalement le traitement ! Un dosage des hormones thyroïdiennes par prise de sang permettra de voir si, effectivement, il y a un déséquilibre. Dans ce cas, un ajustement suffira sans doute à rétablir la situation.
Par ailleurs, un signalement de pharmacovigilance, soit par le médecin, soit par le patient directement, est indispensable. La procédure est accessible par Internet, via le site de l’ANSM (1). Attention, il faut être en mesure de fournir un dosage postérieur au changement de formule.
(1) http://ansm.sante.fr/Declarer-un-effet-indesirable/Votre-declaration-concerne-un-medicament/Votre-declaration-concerne-un-medicament/
Anne-Sophie Stamane
Lire aussi